杭州医学所谭蔚泓院士与邱丽萍研究员团队,在阿尔茨海默病(AD)治疗领域取得重要研究进展。他们成功开发了一种基于核酸适体的单核细胞疗法,该疗法能够高效清除AD脑内的致病性蛋白Tau,为这一困扰全球的神经退行性疾病提供了新的治疗策略。相关研究以“Targeted clearance of extracellular Tau using aptamer-armed monocytes alleviates neuroinflammation in mice with Alzheimer’s disease”为标题,发表在《Nature Biomedical Engineering》上。
阿尔茨海默病是最常见的老年痴呆症类型,主要表现为记忆和认知功能的逐渐丧失。随着全球人口老龄化加剧,其患病率持续攀升。然而,目前尚无能够有效预防或缓解AD病程的疗法。大量研究表明,细胞外的Tau蛋白会以类似朊病毒的方式在神经网络中扩散,引发连锁性的神经元损伤,这可能是推动AD病情恶化的关键因素。尽管靶向胞外Tau蛋白的疗法颇具潜力,但其发展仍面临巨大挑战:一是受血脑屏障所限,药物入脑效率低;二是对Tau蛋白的清除能力有待提升。因此,开发能够有效干预Tau蛋白相关病理过程的新疗法迫在眉睫。
该研究团队另辟蹊径,通过非基因编辑手段,将一种对Tau蛋白具有高亲和力的核酸适体“安装”在单核细胞表面,构建了一套强大的清除系统。研究人员证实,经过功能化改造的单核细胞能够主动进入并富集于AD模型小鼠的大脑中(包括Tau蛋白沉积严重的区域,如海马体和纹状体等),并结合核酸适体对Tau蛋白的特异性分子识别,能够高效地吞噬脑脊液中的Tau蛋白。
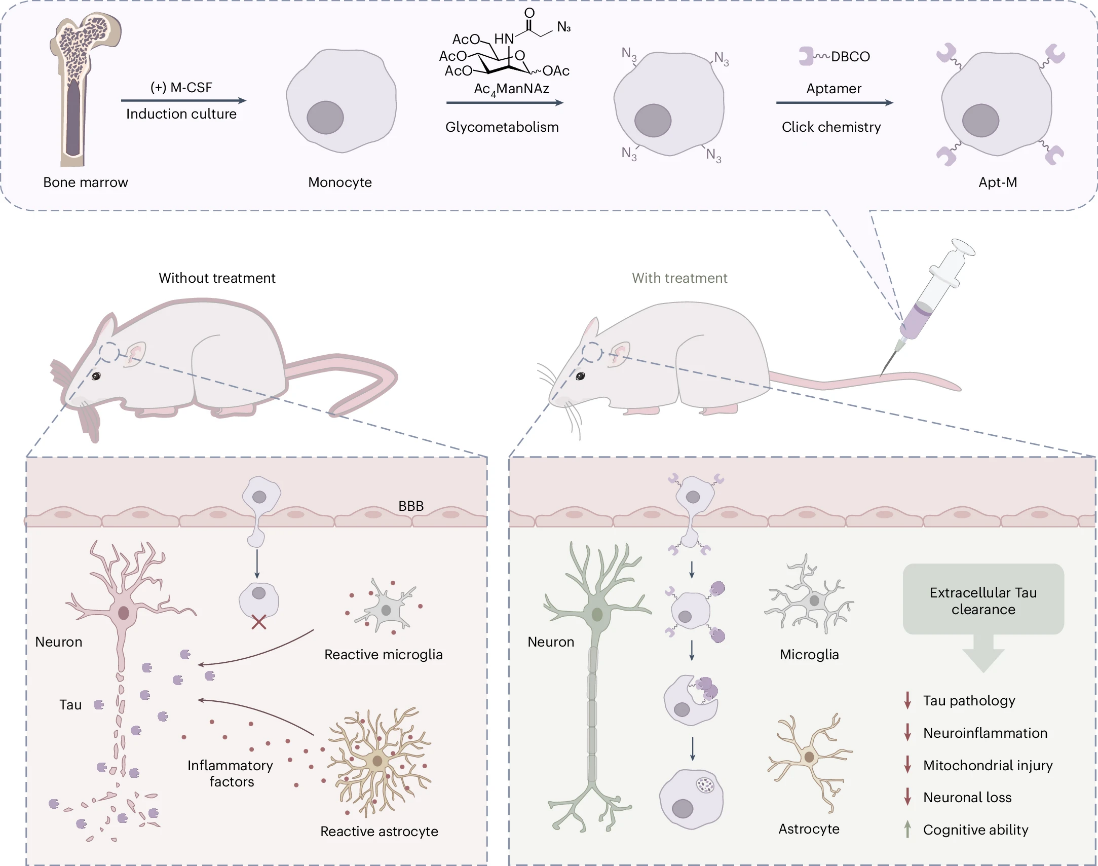
Figure 1. 基于核酸适体的单核细胞疗法工作原理
这一干预措施产生了多重积极效果:它有效抑制了小胶质细胞和星形胶质细胞的过度活化,减轻了神经炎症,并保护了神经元和线粒体的完整性。无论是短期还是长期治疗,均能改善模型小鼠的记忆力和空间学习能力,且未观察到毒性或行为方面的副作用。
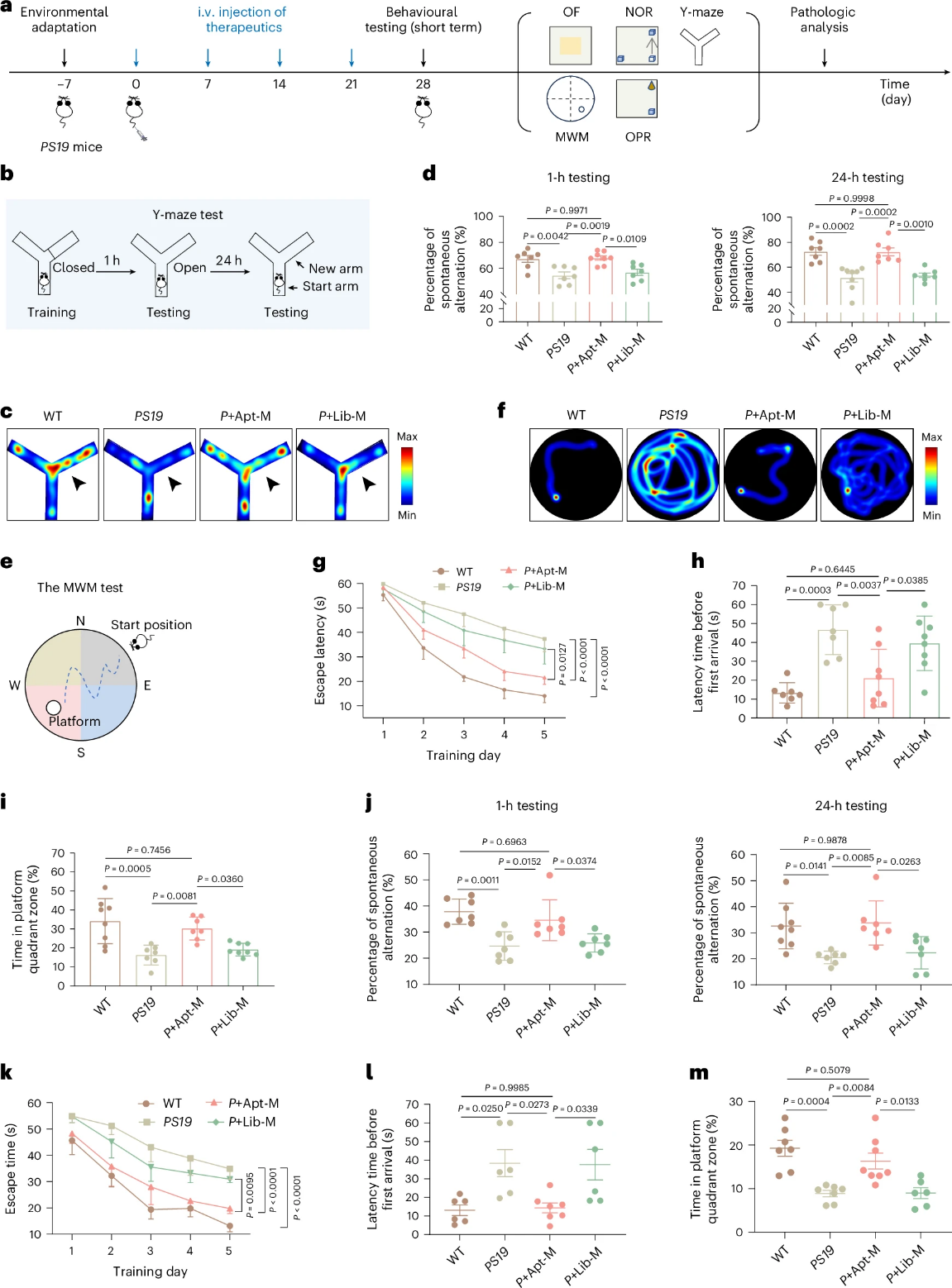
Figure 2. 基于核酸适体的单核细胞疗法显著改善AD小鼠的记忆与认知
该项研究成果表明,基于核酸适体的单核细胞疗法能够在AD患病大脑中实现靶向递送、有效清除和持续的神经保护作用,为阿尔茨海默病的治疗干预提供了一种颇具前景的新策略。
论文链接:https://www.nature.com/articles/s41551-025-01525-2
附件下载:
