背景介绍
围绕环状单链DNA(circular single-stranded DNA, Css DNA)这一分子生物学新工具,中国科学院杭州医学研究所宋杰课题组先前在Nature Communications及Science Advances上发表三篇文章分别从无细胞体系(Nature Communications 2024,15, 4635)和细胞体系(Nature Communications 2023,14,6665;Science Advances. 2025, 11,eadv3396)阐述环状单链 DNA 的蛋白表达机制及调控思路。
传统核酸药物载体在基因治疗各有局限,常见的质粒DNA(pDNA)因含有细菌骨架序列和未甲基化CpG基序,易被先天免疫系统识别清除,引发炎症反应。mRNA载体虽免疫原性较低,但半衰期短,难以维持长效治疗。针对需要长效蛋白补充的疾病以及肿瘤治疗性疫苗的治疗需求,理想的基因表达载体应当同时具备低免疫原性与长效表达的特点,以克服现有技术的局限。近年来,Css DNA作为一种新型基因表达载体进入研究者视野。Css DNA的单链结构去除了冗余序列,可有效避免激活cGAS-STING通路,从而减少先天免疫识别。近期,宋杰课题组在Molecular Therapy、Advanced Healthcare Materials和Journal of Nanobiotechnology上连续发表三篇文章,在动物体系发现了Css DNA低免疫原性和长效表达的特点。文章进一步阐述了Css DNA用于肿瘤疫苗及免疫治疗的潜能,为下一代肿瘤疫苗和免疫治疗提供了全新的载体平台。
研究内容
一. “天然”低免疫原性
首先,研究团队系统比较了Css DNA与pDNA的免疫原性差异。将EGFP编码的Css DNA与pDNA分别包封于脂质纳米颗粒(LNP)中,经静脉注射至小鼠体内。结果显示,pDNA-LNP组小鼠血清中IL-6、IFN-γ、IFN-β等炎症因子水平急剧升高,提示其激活了强烈的先天免疫反应;而Css DNA-LNP组上述炎症因子仅微弱上升,与空载LNP对照组无显著差异。进一步分析发现,Css DNA处理组小鼠血清中IL-1受体拮抗剂(IL-1RA)特异性上调,提示机体可能启动了负反馈机制以抑制残余炎症。在高剂量毒性实验中,pDNA-LNP组小鼠死亡率达40%,并出现严重肝损伤;而Css DNA-LNP组无死亡,仅见轻微转氨酶升高,组织病理学检查未见明显炎性浸润。机制研究表明,单链结构的Css DNA无法有效结合cGAS且去除了冗余序列,这是其低免疫原性的分子基础。
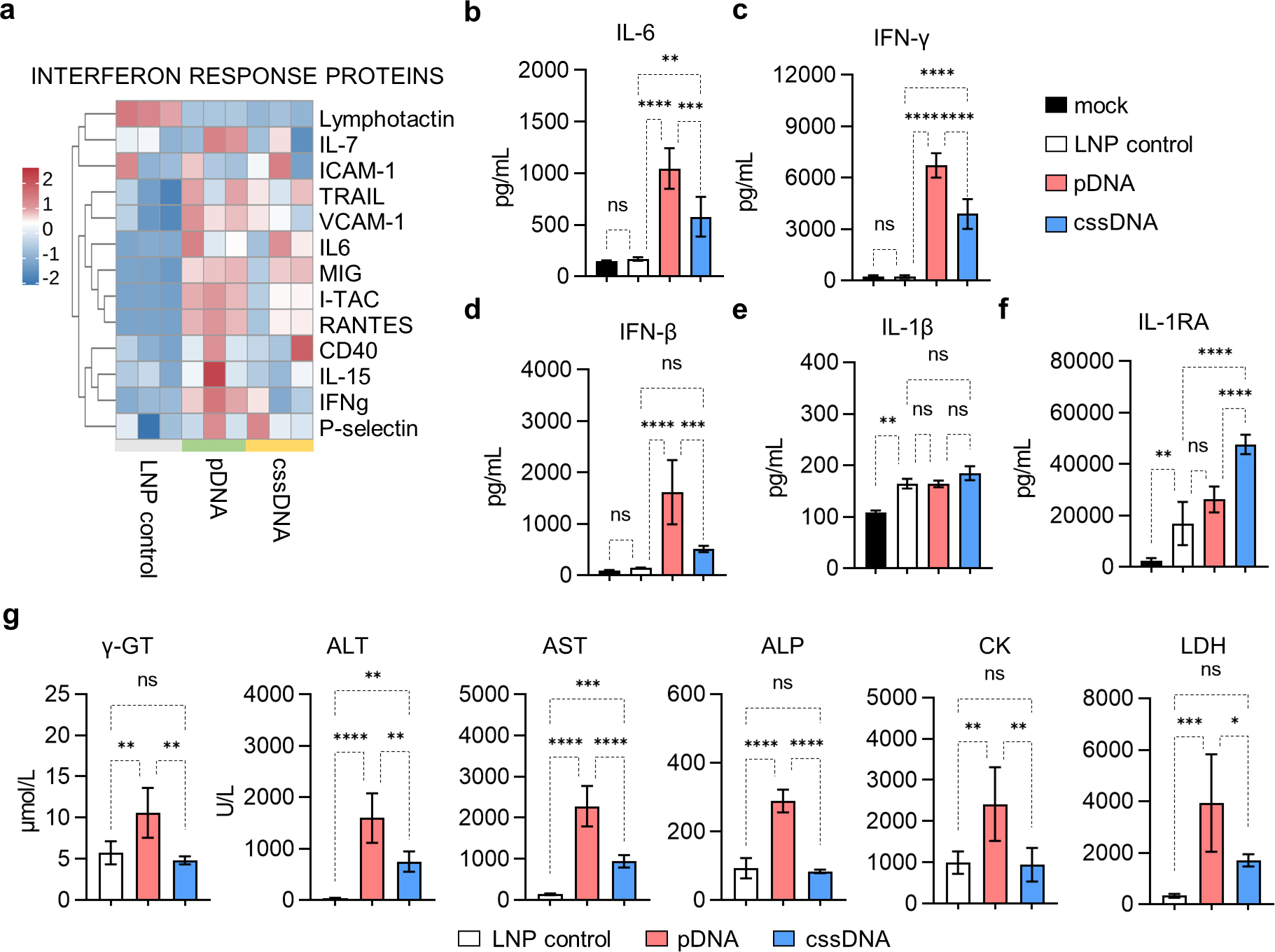
图1. Css DNA与pDNA的免疫原性比较
二. 长效稳定表达
此外,采用体内电转染技术,将携带荧光素酶报告基因的Css DNA(Css Luc)和传统质粒DNA(pDNA)分别导入小鼠肌肉组织。活体成像结果显示,pDNA组的荧光信号在28天后明显衰减,而Css DNA组至少在315天内维持了稳定表达,表达强度比pDNA组高出近10倍。这种长效稳定表达的机制可能有两方面原因:一是Css DNA不含细菌骨架,避免了异染色质介导的基因沉默;二是其单链结构不易被cGAS-STING通路识别,减少了在细胞内的清除,从而延长了半衰期。
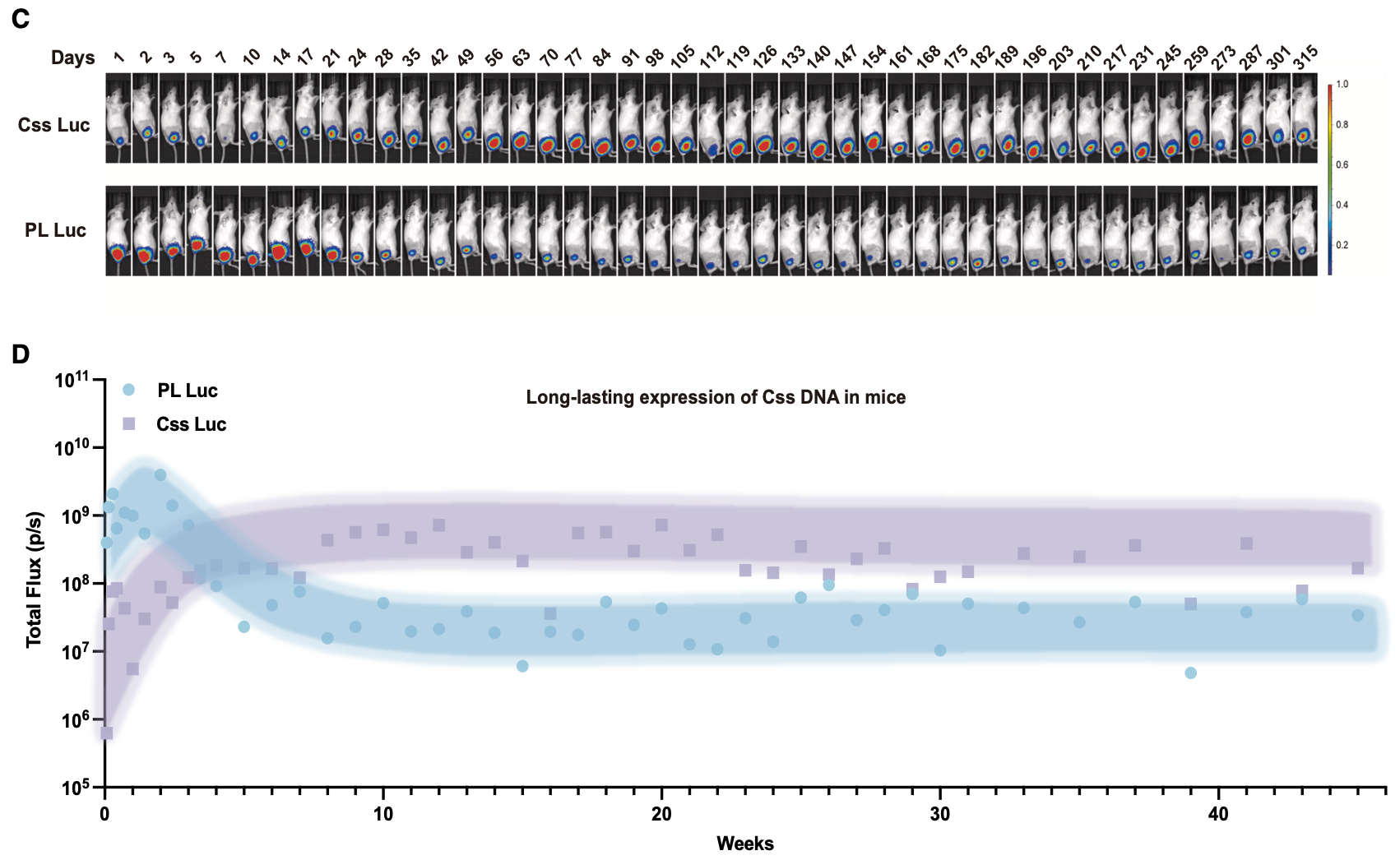
图2. Css DNA与pDNA在小鼠肌肉中的长效表达比较
三. 基于Css DNA的肿瘤疫苗及免疫治疗
为评估Css DNA在肿瘤疫苗的应用潜力,研究团队选用卵清蛋白(OVA)作为模式抗原,构建了Css OVA疫苗,并在B16-OVA黑色素瘤和E.G7-OVA淋巴瘤模型中验证其预防与治疗效果。单次接种90天后,Css OVA组仍有5/8小鼠未成瘤,而pDNA对照组小鼠全部发生肿瘤。进一步将Css OVA与Css IL-12联合用于治疗性疫苗接种,结果显示,联合治疗组小鼠肿瘤生长显著减缓,中位生存期延长2倍以上。
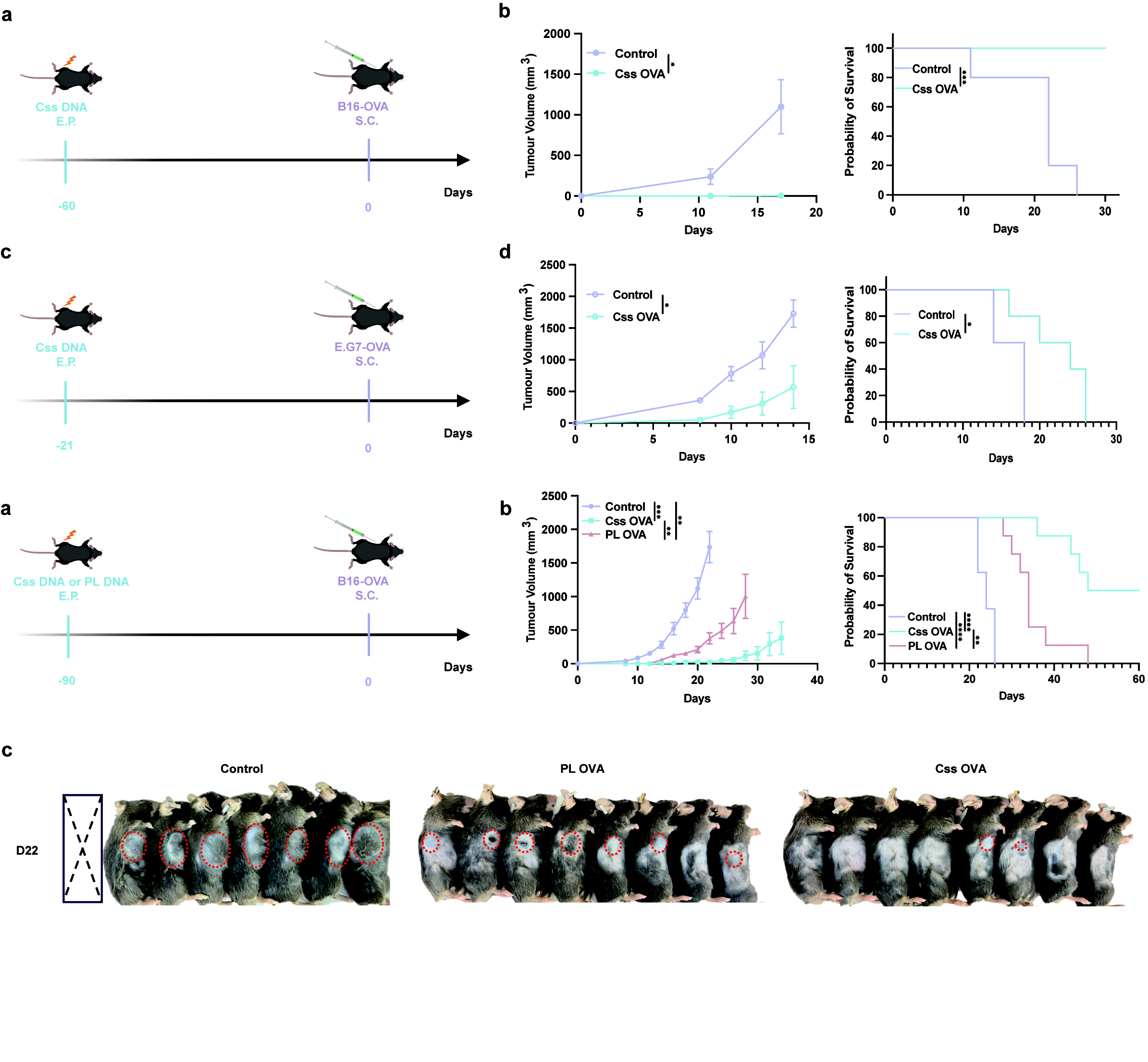
图3. Css OVA肿瘤疫苗的长期预防
此外,在c-MYC/p53原发性肝癌模型中验证Css IL-12-LNP治疗效果。静脉注射Css IL-12-LNP后,肿瘤组织中检测到IL-12高表达,CD3⁺、CD4⁺、CD8⁺ T细胞浸润显著增加,肿瘤重量较对照组减轻70%以上。安全性评估显示,Css DNA组非肿瘤肝组织仅出现轻微炎症反应,而pDNA组则观察到明显的肝细胞损伤和炎性浸润,再次验证Css DNA的安全性优势。
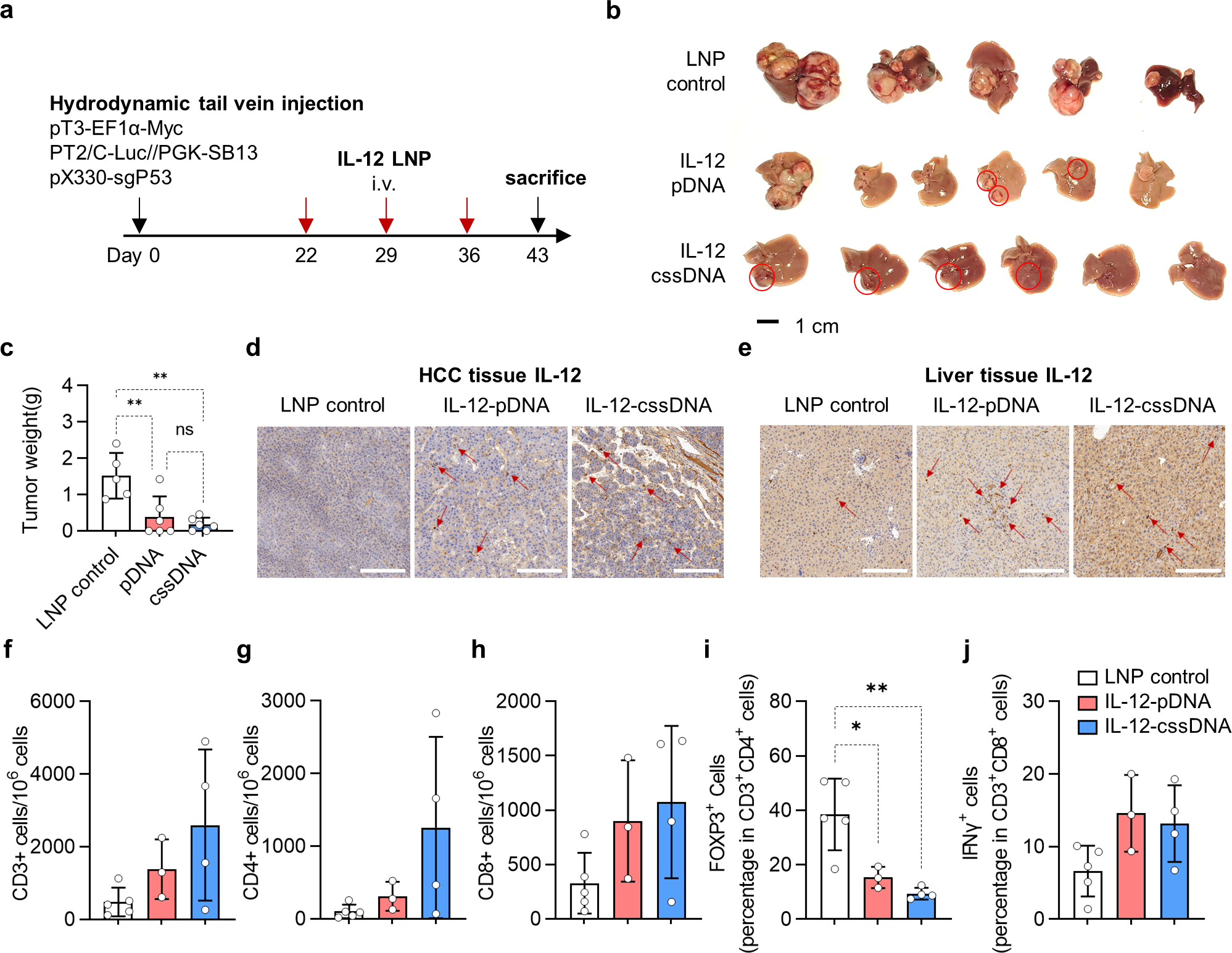
图4. Css IL-12-LNP在原发性肝癌模型中的疗效
研究团队进一步探索了瘤内注射作为递送途径的可行性。在Hepa1-6小鼠肝癌皮下模型及4T1三阴性乳腺癌模型中,Css IL-12 LNP瘤内注射展现出显著治疗效果。Css IL-12 LNP组肿瘤生长受到明显抑制,部分小鼠实现肿瘤完全消退,而空载LNP对照组小鼠全部死亡。相比之下,质粒IL-12 LNP组虽也有完全缓解的个例,但肿瘤抑制速度和生存获益均略逊于Css组。在此基础上,研究团队尝试通过叶酸修饰构建靶向LNP(FA-LNP),以实现静脉注射后的主动递送。结果显示,FA-IL-12-LNP治疗组的肿瘤抑制效果显著优于非靶向对照组。
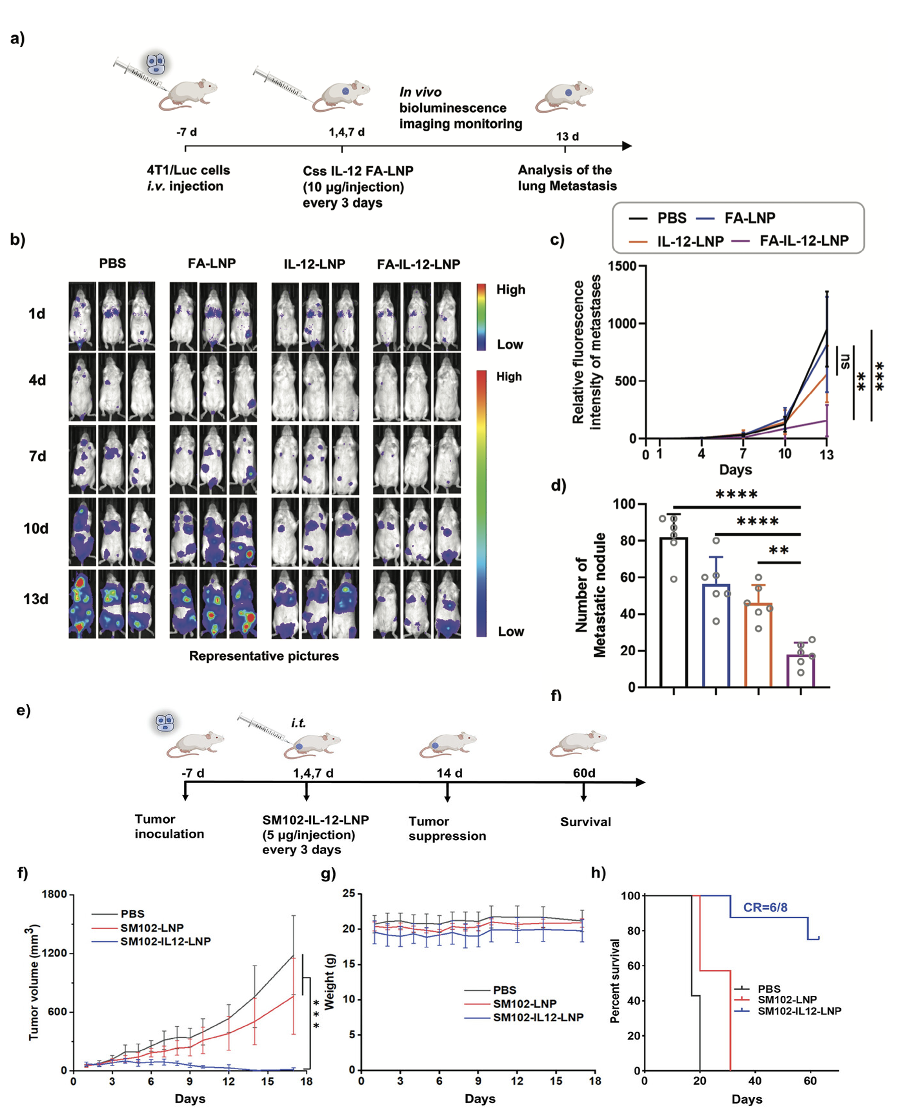
图5. 瘤内注射与主动靶向Css IL-12 LNP的疗效
总结与展望
宋杰课题组围绕Css DNA开展的三篇动物体内研究,系统验证了Css DNA作为新型基因载体的核心优势:(1) 低免疫原性。Css DNA的单链结构可规避cGAS-STING通路的识别,加之不含冗余序列,显著降低了炎症反应,安全性优于传统pDNA。(2) 长效稳定表达。单次给药可在体内维持稳定表达至少300天,效果远超mRNA与pDNA,尤其适用于需长期补充蛋白的疾病治疗。(3) 广泛的肿瘤适应性。在肝癌、三阴性乳腺癌、黑色素瘤及淋巴瘤等多种模型中均验证了其治疗潜力,既可构建治疗性疫苗,亦可作为免疫增敏剂联合应用。(4) 灵活的给药方式。支持瘤内注射与静脉注射,适配不同临床需求。。
未来Css DNA平台可进一步拓展至蛋白替代疗法、罕见病基因治疗等领域。其程序化设计和易于规模化生产的特性,使其具备良好的临床转化前景。
参考文献
- Zhang Y, Cao X, Hu G, et al. Targeted Delivery of Circular Single-Stranded DNA Encoding IL-12 for the Treatment of Triple-Negative Breast Cancer. Advanced Healthcare Materials. 2024;13(29):2401376.
- Liu R, Ye R, Hu G, et al. Antigen-encoding circular single-stranded DNA for cancer vaccine. Molecular Therapy. 2026; In press.
- Hu G, Ye R, Li Z, et al. Interleukin-12 expressing circular single-stranded DNA lipid nanoparticles reprograms the immunosuppressive tumor microenvironment of hepatocellular carcinoma. Journal of Nanobiotechnology. 2026.
附件下载:
